żĂÇŘ Ăą °Ç°ş¸Çč˝É»çĆň°ˇżř ľŕÁ¦±Ţż©Ćň°ˇŔ§żřȸ(ľŕĆňŔ§)żˇĽ 3ÁľŔÇ Ç׾ĎÁ¦°ˇ ±Ţż© 8şÎ ´ÉĽ±Ŕ» łŃľú´Ů.
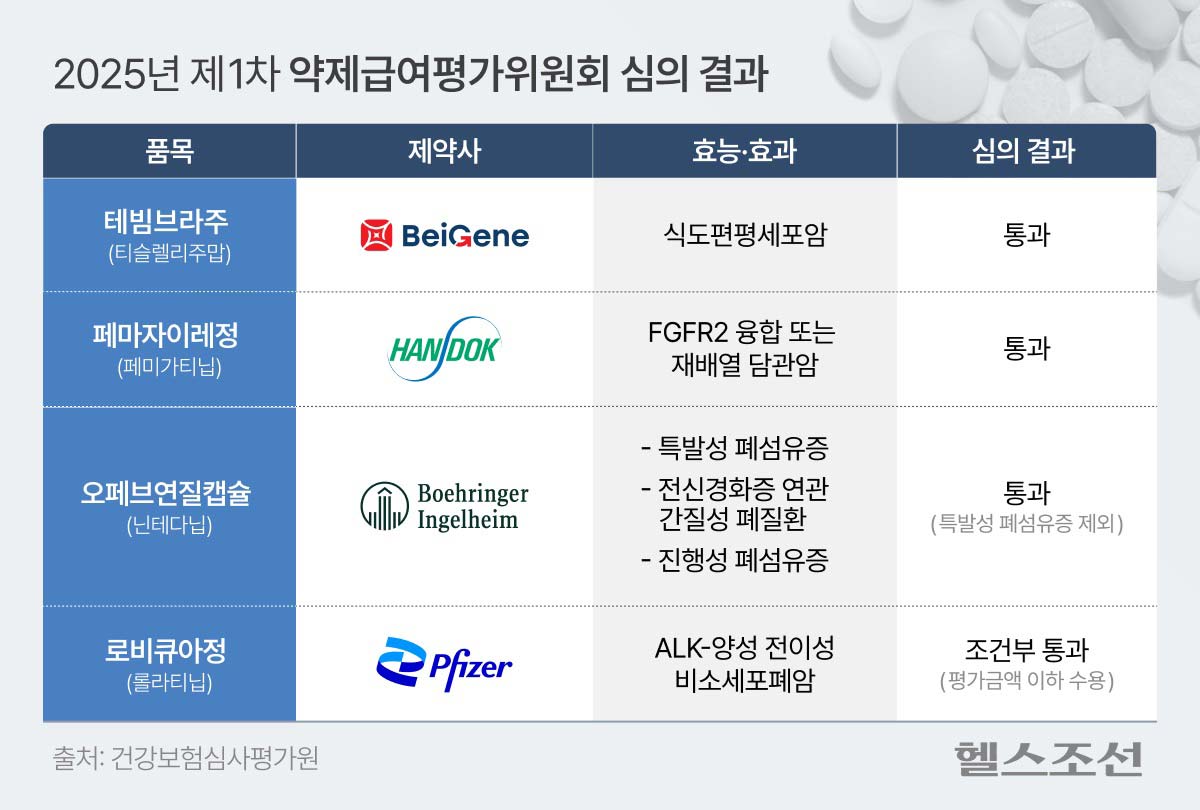
ľŕĆňŔ§´Â ˝ĹľŕŔ» ş¸ŔŻÇŃ Á¦ľŕ»ç°ˇ ±Ţż© µîŔ縦 ˝ĹĂ»ÇŃ Čż´Éˇ¤Čż°ú(ŔűŔŔÁő)żˇ ´ëÇŘ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÖ´ÂÁö Ćň°ˇÇĎ´Â ´Ü°č´Ů. ŔĚąř ľŕĆňŔ§żˇĽ´Â şŁŔĚÁřŔÇ ˝ÄµµľĎ ġ·áÁ¦ 'Ĺ׺öşę¶ó'°ú Çѵ¶ŔÇ °Łł» ´ă°üľĎ ġ·áÁ¦ 'Ć丶ŔÚŔĚ·ą', şŁ¸µ°ĹŔΰÖÇĎŔÓŔÇ ĆóĽ¶ŔŻÁő ġ·áÁ¦ 'żŔĆäşę(ĆŻąßĽş ĆóĽ¶ŔŻÁő Á¦żÜ)'°ˇ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÎÁ¤µĆ´Ů. ľŕĆňŔ§¸¦ łŃŔş ľŕÁ¦´Â ÇâČÄ ±ąąÎ°Ç°ş¸Çč°ř´Ü°úŔÇ ľŕ°ˇ Çů»ó°ú ş¸°ÇşąÁöşÎ °Ç°ş¸ÇčÁ¤ĂĄ˝ÉŔÇŔ§żřȸ(°ÇÁ¤˝É)Ŕ» Ĺë°úÇĎ¸é ±Ţż© ¸ń·Ďżˇ żŔ¸Ą´Ů.
ˇŢĹ׺öşę¶óˇ¤Ć丶ŔÚŔĚ·ą, ±Ţż© ŔűÁ¤Ľş ŔÎÁ¤
ÁöłÇŘ 8żů ˝ÉĆňżř ľĎÁúČŻ˝ÉŔÇŔ§żřȸ(ľĎÁú˝É)Ŕ» Ĺë°úÇŃ 2ÁľŔÇ Ç׾ĎÁ¦°ˇ ±Ţż© 8şÎ ´ÉĽ±Ŕ» łŃľú´Ů. şŁŔĚÁřŔÇ ¸éżŞÇ׾ĎÁ¦ 'Ĺ׺öşę¶ó(ĽşşĐ¸í ĆĽ˝˝·Ľ¸®ÁÖ¸ż)'żÍ Çѵ¶ŔÇ °Łł» ´ă°üľĎ ġ·áÁ¦ 'Ć丶ŔÚŔĚ·ą(ĽşşĐ¸í ĆäąĚ°ˇĆĽ´Ő)'°ˇ ÁÖŔΰřŔĚ´Ů.
Ĺ׺öşę¶ó´Â ¸éżŞ°üą® ĽöżëĂĽŔÎ PD-1żˇ °áÇŐÇĎ´Â ´ÜŬ·ĐÇ×ĂĽ·Î, ±ął»żˇĽ´Â Áöł 2023łâ 11żů ˝ÄµµĆíĆňĽĽĆ÷ľĎ(˝ÄµµľĎ) ġ·áÁ¦·Î Çă°ˇµĆ´Ů. ±¸ĂĽŔűŔÎ ŔűŔŔÁőŔş ŔĚŔü ąé±Ý ±âąÝ ČÇĐżäąý ġ·á¸¦ ÁöĽÓÇŇ Ľö ľř°ĹłŞ Ĺőż© ŔĚČÄżˇ Ŕçąß ¶Ç´Â ÁřÇŕµČ ŔýÁ¦ şŇ°ˇ´É, ŔçąßĽş, ±ąĽŇ ÁřÇ༺ ¶Ç´Â ŔüŔĚĽş ˝ÄµµĆíĆňĽĽĆ÷ľĎ ĽşŔÎ ČŻŔÚżˇĽŔÇ ´Üµ¶żäąýŔĚ´Ů.
ľŕĆňŔ§´Â ˝ĹľŕŔ» ş¸ŔŻÇŃ Á¦ľŕ»ç°ˇ ±Ţż© µîŔ縦 ˝ĹĂ»ÇŃ Čż´Éˇ¤Čż°ú(ŔűŔŔÁő)żˇ ´ëÇŘ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÖ´ÂÁö Ćň°ˇÇĎ´Â ´Ü°č´Ů. ŔĚąř ľŕĆňŔ§żˇĽ´Â şŁŔĚÁřŔÇ ˝ÄµµľĎ ġ·áÁ¦ 'Ĺ׺öşę¶ó'°ú Çѵ¶ŔÇ °Łł» ´ă°üľĎ ġ·áÁ¦ 'Ć丶ŔÚŔĚ·ą', şŁ¸µ°ĹŔΰÖÇĎŔÓŔÇ ĆóĽ¶ŔŻÁő ġ·áÁ¦ 'żŔĆäşę(ĆŻąßĽş ĆóĽ¶ŔŻÁő Á¦żÜ)'°ˇ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÎÁ¤µĆ´Ů. ľŕĆňŔ§¸¦ łŃŔş ľŕÁ¦´Â ÇâČÄ ±ąąÎ°Ç°ş¸Çč°ř´Ü°úŔÇ ľŕ°ˇ Çů»ó°ú ş¸°ÇşąÁöşÎ °Ç°ş¸ÇčÁ¤ĂĄ˝ÉŔÇŔ§żřȸ(°ÇÁ¤˝É)Ŕ» Ĺë°úÇĎ¸é ±Ţż© ¸ń·Ďżˇ żŔ¸Ą´Ů.
ˇŢĹ׺öşę¶óˇ¤Ć丶ŔÚŔĚ·ą, ±Ţż© ŔűÁ¤Ľş ŔÎÁ¤
ÁöłÇŘ 8żů ˝ÉĆňżř ľĎÁúČŻ˝ÉŔÇŔ§żřȸ(ľĎÁú˝É)Ŕ» Ĺë°úÇŃ 2ÁľŔÇ Ç׾ĎÁ¦°ˇ ±Ţż© 8şÎ ´ÉĽ±Ŕ» łŃľú´Ů. şŁŔĚÁřŔÇ ¸éżŞÇ׾ĎÁ¦ 'Ĺ׺öşę¶ó(ĽşşĐ¸í ĆĽ˝˝·Ľ¸®ÁÖ¸ż)'żÍ Çѵ¶ŔÇ °Łł» ´ă°üľĎ ġ·áÁ¦ 'Ć丶ŔÚŔĚ·ą(ĽşşĐ¸í ĆäąĚ°ˇĆĽ´Ő)'°ˇ ÁÖŔΰřŔĚ´Ů.
Ĺ׺öşę¶ó´Â ¸éżŞ°üą® ĽöżëĂĽŔÎ PD-1żˇ °áÇŐÇĎ´Â ´ÜŬ·ĐÇ×ĂĽ·Î, ±ął»żˇĽ´Â Áöł 2023łâ 11żů ˝ÄµµĆíĆňĽĽĆ÷ľĎ(˝ÄµµľĎ) ġ·áÁ¦·Î Çă°ˇµĆ´Ů. ±¸ĂĽŔűŔÎ ŔűŔŔÁőŔş ŔĚŔü ąé±Ý ±âąÝ ČÇĐżäąý ġ·á¸¦ ÁöĽÓÇŇ Ľö ľř°ĹłŞ Ĺőż© ŔĚČÄżˇ Ŕçąß ¶Ç´Â ÁřÇŕµČ ŔýÁ¦ şŇ°ˇ´É, ŔçąßĽş, ±ąĽŇ ÁřÇ༺ ¶Ç´Â ŔüŔĚĽş ˝ÄµµĆíĆňĽĽĆ÷ľĎ ĽşŔÎ ČŻŔÚżˇĽŔÇ ´Üµ¶żäąýŔĚ´Ů.
Ĺ׺öşę¶ó´Â ŔŰłâ 3żů ľĎÁú˝ÉŔ» ÇŃ Â÷·Ę Ĺë°úÇĎÁö ¸řÇßŔ¸łŞ, ŔçµµŔü łˇżˇ ŔŰłâ 8żů ±Ţż© ±âÁŘŔ» ĽłÁ¤ÇĎ´Â µĄ Ľş°řÇß´Ů. ŔĚąř ľŕĆňŔ§żˇĽ´Â ˝ÄµµĆíĆňĽĽĆ÷ľĎ ġ·áÁ¦·Î ±Ţż© ŔűÁ¤ĽşŔĚ ŔÎÁ¤µĆ´Ů.
Ć丶ŔÚŔĚ·ą´Â ĽĽĆ÷ŔÇ ĽşŔĺ°ú şĐČżˇ °üż©ÇĎ´Â Ľ¶ŔŻľĆĽĽĆ÷ĽşŔĺŔÎŔÚ ĽöżëĂĽ2(FGFR2) Ŕ¶ÇŐˇ¤Ŕçąčż·Î ŔÎÇŘ ąß»ýÇŃ ľĎĽĽĆ÷ŔÇ Áő˝ÄŔ» ľďÁ¦ÇĎ´Â ¸Ô´Â FGFR ľďÁ¦Á¦·Î, Áöł 2023łâ 4żů ±ął» Çă°ˇ¸¦ ČąµćÇß´Ů. Ľ¶ŔŻľĆĽĽĆ÷ĽşŔĺŔÎŔÚ ĽöżëĂĽ¶ő ĽĽĆ÷¸· ĽöżëĂĽ·Î ĽĽĆ÷ ĽşŔĺ, »ýÁ¸°ú şĐȸ¦ Á¶ŔýÇĎ´Â żŞÇŇŔ» Çϸç, ŔĚ ĽöżëĂĽżˇ µąż¬şŻŔĚ°ˇ »ý±â¸é ľĎŔĚ ąß»ýÇŃ´Ů. ÇöŔç ±ął»żˇĽ Ć丶ŔÚŔĚ·ą´Â 1ȸ ŔĚ»óŔÇ Ŕü˝Ĺ ġ·á¸¦ ąŢŔş FGFR2 Ŕ¶ÇŐ ¶Ç´Â ŔçąčżŔĚ ŔÖ´Â ĽşŔÎ ±ąĽŇ ÁřÇ༺ˇ¤ŔüŔĚĽş ´ă°üľĎ ČŻŔÚżˇ°Ô »çżëÇŇ Ľö ŔÖ´Ů.
Ć丶ŔÚŔĚ·ą ¶ÇÇŃ 2ąřŔÇ µµŔü łˇżˇ ŔŰłâ 8żů ľĎÁú˝ÉŔÇ ą®ĹÎŔ» łŃľúŔ¸¸ç, ˝ÉĆňżřŔş ŔĚąř ľŕĆňŔ§żˇĽ FGFR2 Ŕ¶ÇŐ ¶Ç´Â Ŕçąčż ´ă°üľĎ ŔűŔŔÁőżˇ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÖ´Ů°í ĆÇ´ÜÇß´Ů.
ˇŢżŔĆäşę, 'ĆŻąßĽş ĆóĽ¶ŔŻÁő'Ŕş şń±Ţż©ˇ¦ ·ÎşńĹĄľĆ, ľŕ°ˇ ą®Á¦ ÇŘ°á ÇĘżä
şŁ¸µ°ĹŔΰÖÇĎŔÓŔÇ 'żŔĆäşę(ĽşşĐ¸í ´ŃĹ×´Ů´Ő)'´Â ŔĚ´Ţ 25ŔĎ ą°ÁúĆŻÇă ¸¸·á¸¦ ľŐµĐ ĆóĽ¶ŔŻÁő ġ·áÁ¦´Ů. 2016łâ ±ął»żˇĽ ĆŻąßĽş ĆóĽ¶ŔŻÁő ġ·áÁ¦·Î Çă°ˇąŢŔş ŔĚČÄ Ŕü˝Ĺ°ćČÁő ż¬°ü °ŁÁúĽş ĆóÁúČŻ ČŻŔÚŔÇ Ćó ±â´É °¨ĽŇ Áöż¬°ú 2016łâ ĆŻąßĽş ĆóĽ¶ŔŻÁőŔ¸·Î Çă°ˇ¸¦ ąŢŔş µĄ ŔĚľî 'Ŕü˝Ĺ°ćČÁő ż¬°ü °ŁÁúĽş ĆóÁúČŻ°ú ÁřÇ༺ ĆóĽ¶ŔŻÁőżˇµµ ŔűŔŔÁőŔ» łĐÇű´Ů. ´Ů¸¸, ´ëĂĽÁ¦ŔÎ ŔϵżÁ¦ľŕŔÇ 'ÇÇ·ą˝şĆÄ(ĽşşĐ¸í ÇǸŁĆä´Ďµ·)'żÍŔÇ ľŕ°ˇ Â÷ŔĚ°ˇ ÁöŔűµÇ¸éĽ ±Ţż©°ˇ Áöż¬µĆ´Ů.
ŔĚąř ľŕĆňŔ§żˇĽ żŔĆäşę´Â ˇăŔü˝Ĺ°ćČÁő ż¬°ü °ŁÁúĽş ĆóÁúČŻ°ú ˇăÁřÇ༺ ĆóĽ¶ŔŻÁőżˇ ´ëÇŘ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÎÁ¤µČ ąÝ¸é, ĆŻąßĽş ĆóĽ¶ŔŻÁőżˇ ´ëÇŘĽ´Â ŔÎÁ¤µÇÁö ľĘľŇ´Ů.
ľŕ°ˇ °ü·Ă Á¶°ÇşÎ ŔÎÁ¤Ŕ» ąŢŔş ľŕÁ¦µµ ŔÖ´Ů. ÇѱąČŔĚŔÚÁ¦ľŕŔÇ '·ÎşńĹĄľĆ(ĽşşĐ¸í ·Ń¶óĆĽ´Ő)'´Â żŞÇüĽş ¸˛ÇÁÁľ ŔλęČČżĽŇ(ALK) ľçĽş ŔüŔĚĽş şńĽŇĽĽĆ÷ĆóľĎ ġ·áÁ¦·Î ±Ţż© ąüŔ§ Č®´ëżˇ łŞĽąŔ¸łŞ, ľŕ°ˇ ŔÎÇĎ ľĐąÚŔ» ąŢ°í ŔÖ´Â °ÍŔ¸·Î łŞĹ¸łµ´Ů. ľŕĆňŔ§´Â ·ÎşńĹĄľĆżˇ ´ëÇŘ Ćň°ˇ ±Ýľ× ŔĚÇϸ¦ ĽöżëÇŇ °ćżě ±Ţż© ąüŔ§ Č®´ëżˇ ŔűÁ¤ĽşŔĚ ŔÖ´Ů°í ĆÇ´ÜÇß´Ů.
·ÎşńĹĄľĆ´Â 2ĽĽ´ë ġ·áÁ¦ Ĺőż© ČÄ °ˇŔĺ ¸ąŔĚ ąß»ýÇĎ´Â ALK G1202R, I1171T şŻŔĚ µî ±¤ąüŔ§ÇŃ ALK ł»Ľş şŻŔ̸¦ ľďÁ¦ÇĎ´Â 3ĽĽ´ë ALK ĆĽ·Î˝Ĺ Ĺ°łŞÁ¦ ľďÁ¦Á¦(TKI)·Î, łú-Ç÷ľ×Ŕĺş®(BBB) Ĺë°ú°ˇ żëŔĚÇϵµ·Ď Ľł°čµĹ łúŔüŔĚ ČŻŔÚżˇ°Ôµµ żěĽ±ŔűŔ¸·Î °í·ÁµÇ´Â ľŕÁ¦´Ů. ŔÓ»ó 3»ó ˝ĂÇč 'CROWN'żˇĽ ALK ľçĽş şńĽŇĽĽĆ÷ĆóľĎ ČŻŔÚŔÇ 5łâ ą«ÁřÇŕ »ýÁ¸Ŕ˛(PFS)ŔĚ 60%·Î łŞĹ¸łŞ´Â µî Čż´ÉŔĚ ĂćşĐČ÷ ŔÔÁőµĆŔ¸łŞ, ľŕ°ˇ ą®Á¦°ˇ ąß¸ńŔ» Ŕâ°í ŔÖ´Ů. ÇѱąČŔĚŔÚÁ¦ľŕŔş ŔŰłâ 5żů ±ąąÎ°Ç°ş¸Çč°ř´Ü°úŔÇ ·ÎşńĹĄľĆ ľŕ°ˇ Çů»óżˇĽµµ ÇŐŔÇżˇ Ŕ̸ŁÁö ¸řÇŘ ľĎÁú˝É ´Ü°čşÎĹÍ ´Ů˝Ă °ĹĂĆŔ¸¸ç, ŔĚąř ľŕĆňŔ§żˇĽµµ 'Ćň°ˇ±Ýľ× ŔĚÇĎ Ľöżë'Ŕ̶ó´Â Á¶°ÇŔĚ µű¶óşŮľú´Ů.
Ć丶ŔÚŔĚ·ą´Â ĽĽĆ÷ŔÇ ĽşŔĺ°ú şĐČżˇ °üż©ÇĎ´Â Ľ¶ŔŻľĆĽĽĆ÷ĽşŔĺŔÎŔÚ ĽöżëĂĽ2(FGFR2) Ŕ¶ÇŐˇ¤Ŕçąčż·Î ŔÎÇŘ ąß»ýÇŃ ľĎĽĽĆ÷ŔÇ Áő˝ÄŔ» ľďÁ¦ÇĎ´Â ¸Ô´Â FGFR ľďÁ¦Á¦·Î, Áöł 2023łâ 4żů ±ął» Çă°ˇ¸¦ ČąµćÇß´Ů. Ľ¶ŔŻľĆĽĽĆ÷ĽşŔĺŔÎŔÚ ĽöżëĂĽ¶ő ĽĽĆ÷¸· ĽöżëĂĽ·Î ĽĽĆ÷ ĽşŔĺ, »ýÁ¸°ú şĐȸ¦ Á¶ŔýÇĎ´Â żŞÇŇŔ» Çϸç, ŔĚ ĽöżëĂĽżˇ µąż¬şŻŔĚ°ˇ »ý±â¸é ľĎŔĚ ąß»ýÇŃ´Ů. ÇöŔç ±ął»żˇĽ Ć丶ŔÚŔĚ·ą´Â 1ȸ ŔĚ»óŔÇ Ŕü˝Ĺ ġ·á¸¦ ąŢŔş FGFR2 Ŕ¶ÇŐ ¶Ç´Â ŔçąčżŔĚ ŔÖ´Â ĽşŔÎ ±ąĽŇ ÁřÇ༺ˇ¤ŔüŔĚĽş ´ă°üľĎ ČŻŔÚżˇ°Ô »çżëÇŇ Ľö ŔÖ´Ů.
Ć丶ŔÚŔĚ·ą ¶ÇÇŃ 2ąřŔÇ µµŔü łˇżˇ ŔŰłâ 8żů ľĎÁú˝ÉŔÇ ą®ĹÎŔ» łŃľúŔ¸¸ç, ˝ÉĆňżřŔş ŔĚąř ľŕĆňŔ§żˇĽ FGFR2 Ŕ¶ÇŐ ¶Ç´Â Ŕçąčż ´ă°üľĎ ŔűŔŔÁőżˇ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÖ´Ů°í ĆÇ´ÜÇß´Ů.
ˇŢżŔĆäşę, 'ĆŻąßĽş ĆóĽ¶ŔŻÁő'Ŕş şń±Ţż©ˇ¦ ·ÎşńĹĄľĆ, ľŕ°ˇ ą®Á¦ ÇŘ°á ÇĘżä
şŁ¸µ°ĹŔΰÖÇĎŔÓŔÇ 'żŔĆäşę(ĽşşĐ¸í ´ŃĹ×´Ů´Ő)'´Â ŔĚ´Ţ 25ŔĎ ą°ÁúĆŻÇă ¸¸·á¸¦ ľŐµĐ ĆóĽ¶ŔŻÁő ġ·áÁ¦´Ů. 2016łâ ±ął»żˇĽ ĆŻąßĽş ĆóĽ¶ŔŻÁő ġ·áÁ¦·Î Çă°ˇąŢŔş ŔĚČÄ Ŕü˝Ĺ°ćČÁő ż¬°ü °ŁÁúĽş ĆóÁúČŻ ČŻŔÚŔÇ Ćó ±â´É °¨ĽŇ Áöż¬°ú 2016łâ ĆŻąßĽş ĆóĽ¶ŔŻÁőŔ¸·Î Çă°ˇ¸¦ ąŢŔş µĄ ŔĚľî 'Ŕü˝Ĺ°ćČÁő ż¬°ü °ŁÁúĽş ĆóÁúČŻ°ú ÁřÇ༺ ĆóĽ¶ŔŻÁőżˇµµ ŔűŔŔÁőŔ» łĐÇű´Ů. ´Ů¸¸, ´ëĂĽÁ¦ŔÎ ŔϵżÁ¦ľŕŔÇ 'ÇÇ·ą˝şĆÄ(ĽşşĐ¸í ÇǸŁĆä´Ďµ·)'żÍŔÇ ľŕ°ˇ Â÷ŔĚ°ˇ ÁöŔűµÇ¸éĽ ±Ţż©°ˇ Áöż¬µĆ´Ů.
ŔĚąř ľŕĆňŔ§żˇĽ żŔĆäşę´Â ˇăŔü˝Ĺ°ćČÁő ż¬°ü °ŁÁúĽş ĆóÁúČŻ°ú ˇăÁřÇ༺ ĆóĽ¶ŔŻÁőżˇ ´ëÇŘ ±Ţż© ŔűÁ¤ĽşŔĚ ŔÎÁ¤µČ ąÝ¸é, ĆŻąßĽş ĆóĽ¶ŔŻÁőżˇ ´ëÇŘĽ´Â ŔÎÁ¤µÇÁö ľĘľŇ´Ů.
ľŕ°ˇ °ü·Ă Á¶°ÇşÎ ŔÎÁ¤Ŕ» ąŢŔş ľŕÁ¦µµ ŔÖ´Ů. ÇѱąČŔĚŔÚÁ¦ľŕŔÇ '·ÎşńĹĄľĆ(ĽşşĐ¸í ·Ń¶óĆĽ´Ő)'´Â żŞÇüĽş ¸˛ÇÁÁľ ŔλęČČżĽŇ(ALK) ľçĽş ŔüŔĚĽş şńĽŇĽĽĆ÷ĆóľĎ ġ·áÁ¦·Î ±Ţż© ąüŔ§ Č®´ëżˇ łŞĽąŔ¸łŞ, ľŕ°ˇ ŔÎÇĎ ľĐąÚŔ» ąŢ°í ŔÖ´Â °ÍŔ¸·Î łŞĹ¸łµ´Ů. ľŕĆňŔ§´Â ·ÎşńĹĄľĆżˇ ´ëÇŘ Ćň°ˇ ±Ýľ× ŔĚÇϸ¦ ĽöżëÇŇ °ćżě ±Ţż© ąüŔ§ Č®´ëżˇ ŔűÁ¤ĽşŔĚ ŔÖ´Ů°í ĆÇ´ÜÇß´Ů.
·ÎşńĹĄľĆ´Â 2ĽĽ´ë ġ·áÁ¦ Ĺőż© ČÄ °ˇŔĺ ¸ąŔĚ ąß»ýÇĎ´Â ALK G1202R, I1171T şŻŔĚ µî ±¤ąüŔ§ÇŃ ALK ł»Ľş şŻŔ̸¦ ľďÁ¦ÇĎ´Â 3ĽĽ´ë ALK ĆĽ·Î˝Ĺ Ĺ°łŞÁ¦ ľďÁ¦Á¦(TKI)·Î, łú-Ç÷ľ×Ŕĺş®(BBB) Ĺë°ú°ˇ żëŔĚÇϵµ·Ď Ľł°čµĹ łúŔüŔĚ ČŻŔÚżˇ°Ôµµ żěĽ±ŔűŔ¸·Î °í·ÁµÇ´Â ľŕÁ¦´Ů. ŔÓ»ó 3»ó ˝ĂÇč 'CROWN'żˇĽ ALK ľçĽş şńĽŇĽĽĆ÷ĆóľĎ ČŻŔÚŔÇ 5łâ ą«ÁřÇŕ »ýÁ¸Ŕ˛(PFS)ŔĚ 60%·Î łŞĹ¸łŞ´Â µî Čż´ÉŔĚ ĂćşĐČ÷ ŔÔÁőµĆŔ¸łŞ, ľŕ°ˇ ą®Á¦°ˇ ąß¸ńŔ» Ŕâ°í ŔÖ´Ů. ÇѱąČŔĚŔÚÁ¦ľŕŔş ŔŰłâ 5żů ±ąąÎ°Ç°ş¸Çč°ř´Ü°úŔÇ ·ÎşńĹĄľĆ ľŕ°ˇ Çů»óżˇĽµµ ÇŐŔÇżˇ Ŕ̸ŁÁö ¸řÇŘ ľĎÁú˝É ´Ü°čşÎĹÍ ´Ů˝Ă °ĹĂĆŔ¸¸ç, ŔĚąř ľŕĆňŔ§żˇĽµµ 'Ćň°ˇ±Ýľ× ŔĚÇĎ Ľöżë'Ŕ̶ó´Â Á¶°ÇŔĚ µű¶óşŮľú´Ů.
ŔĚ ±â»çżÍ °ü·Ă±â»ç